Калетина Н., Калетин Г. Микроэлементы - биологические регуляторы
Железо и цинк, молибден и селен, медь и кобальт — эти и десятки других химических элементов присутствуют в человеческом организме в минимальных количествах. Однако их влияние на обменные и другие процессы очень велико. И не только их избыток, но и недостаток в органах и тканях приводят к патологиям. Каковы механизмы действия микроэлементов? Почему один и тот же, но в разных дозах и формах, может играть как созидательную, так и разрушительную роль?
МНОГОЛИКИЕ МЕТАЛЛЫ
По словам известного патолога и физиолога академика АМН СССР Александра Авцына (1908-1993), микроэлементы — «скорее всего, не случайные ингредиенты тканей и жидкостей организмов, а компоненты закономерно существующей очень древней и сложной физиологической системы, участвующей в регулировании жизненных функций на всех стадиях развития». В органах и жидкостях человека они распределены неравномерно. Элементы, относящиеся к жизненно необходимым, или эссенциальным (железо, йод, цинк, кобальт, хром, молибден, никель, селен, марганец, фтор, кремний и др.) находятся в значительно больших концентрациях, иногда на несколько порядков, чем токсичные (кадмий, мышьяк, ртуть, сурьма, барий, бор, свинец и т.д.). Их влияние связано не только с количественным фактором, но и в значительной степени с формой элемента: координационно-связанной или ионной.
По словам известного патолога и физиолога академика АМН СССР Александра Авцына (1908-1993), микроэлементы — «скорее всего, не случайные ингредиенты тканей и жидкостей организмов, а компоненты закономерно существующей очень древней и сложной физиологической системы, участвующей в регулировании жизненных функций на всех стадиях развития». В органах и жидкостях человека они распределены неравномерно. Элементы, относящиеся к жизненно необходимым, или эссенциальным (железо, йод, цинк, кобальт, хром, молибден, никель, селен, марганец, фтор, кремний и др.) находятся в значительно больших концентрациях, иногда на несколько порядков, чем токсичные (кадмий, мышьяк, ртуть, сурьма, барий, бор, свинец и т.д.). Их влияние связано не только с количественным фактором, но и в значительной степени с формой элемента: координационно-связанной или ионной.
Напомним: жизнь клетки определяют протеины (белки), в то время как нуклеиновые кислоты представляют только план ее активности. На преобразование белковых молекул влияют разные факторы: приток кислорода, перенесенный стресс, лекарства, пища. Организм все время реагирует на изменения в окружающей среде, пытаясь сохранить физиологическое равновесие. Внешние условия, наоборот, стремятся нарушить его. Поддержание гомеостаза связано с синтезом, преобразованием и разложением белков, а реальную возможность прохождения таких процессов, их направление и скорость определяют ионы металлов. Доказана их роль в процессах роста, дифференцировки, репарации и регенерации, апоптоза, некроза, выживаемости клеток, а также в патогенезе хронических воспалительных и дегенеративных заболеваний.
Приведем несколько примеров, иллюстрирующих разнообразие форм нахождения микроэлементов в живом организме. Скажем, важнейшие железосодержащие белки — это гемопротеины (гемоглобин, миоглобин, цитохромы и др.). Ферментов, содержащих цинк, насчитывается более 200; он входит в структуру тимулина (активного гормона вил очковой железы), участвует в «упаковке» инсулина. Недаром цинк называют еще главным неорганическим гормоном. Медь – кофермент (Коферменты — соединения небелковой природы, входящие в состав некоторых ферментов) дофамин-β-гидроксилазы, без которой не обходится синтез нейромедиаторов. Кобальт — ключевой компонент кофермента витамина В12. Никель обнаружен в гидролитических ферментах человека и в крови в виде комплексов с гистамином и альбуминами. Хорошо известна биологическая роль йода, входящего в состав ряда гормонов.
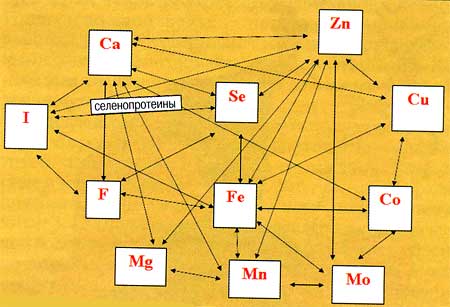
В природе распротранены координированные влияния микроэлементов
Многим живым объектам — от бактерий до человека — свойственно явление биомагнетизма. Магнетит (оксид железа) выполняет функцию их ориентации в магнитном поле Земли и располагается в особых образованиях (магнетосомах), сформированных в виде цепочек по 10-25 кристаллов общей длиной около 50 нм. Недавно немецкие ученые идентифицировали часть ДНК, переносящую полную генетическую информацию, необходимую для образования магнетосомных частиц. В этом фрагменте генома находится, по крайней мере, 25-30 различных магнетосомных генов, чья роль ранее не была известна в деталях.
Каждый элемент имеет присущий ему диапазон безопасной экспозиции, что и обеспечивает оптимальные тканевые концентрации; с другой стороны, у любого из них есть и свой токсический диапазон. Скажем, в давние времена фетр для изготовления шляп обрабатывали солями ртути. Жизнь такого мастера была недолгой и заканчивалась, как правило, психическими расстройствами. Существует даже английская поговорка: «Безумен, как шляпник». Однако хорошо знакома и другая фраза: «Врач, познавший целебные свойства трав и корней, — человек; врач, познавший силу молитвы, — пророк; врач, познавший силу ртути, — Бог». С момента открытия селена (1817 г.) до середины XX в. существовало мнение, что это один из самых токсичных элементов периодической системы Д.И. Менделеева. Но когда в живых организмах и растениях ученые обнаружили природные аминокислоты селеноцистеин и селенометионин, отношение к нему пересмотрели. Тем не менее утверждение «селен токсичен» нельзя признать ошибочным. Но токсичность микроэлемента не исключает эссенциальности.
Один из путей проявления токсичности металлов — конкуренция и замещение жизненно важных катионов, когда на месте «полезного» оказывается «вредный». Например, свинец при определенных условиях заменяет цинк в ферментах, содержащих его, т.е. ингибирует их функцию. Но если принять во внимание, что цинк способствует иммуногенезу, сперматогенезу, репродукции, ранозаживлению, понятно, чем, в особенности детскому организму, грозит загрязненность свинцом, этим «токсикантом №1» окружающей среды. Отравление им может привести к серьезным проблемам обучаемости, нарушениям поведения (агрессивности), перевозбужденности или летаргии. Свинец влияет на кроветворную систему, изменяя активность соответствующих ферментов, вовлеченных в биосинтез генома. Итог — снижение уровня гемоглобина и анемия.
Далее. Дым кальяна, трубки, сигарет содержит значительное количество кадмия — легочного канцерогена. Необратимое неврологическое состояние, близкое к болезни Паркинсона, характеризуемое странным поведением и «маскоподобным» выражением лица, — результат хронического воздействия высоких уровней марганца и часто встречается у подростков-наркоманов, использующих получаемый в домашних условиях эфедрон.
Отметим: в природе распространены координированные влияния нескольких микроэлементов, когда действие одного из них усиливается или подавляется в присутствии другого. Существуют их пары и триады, оказывающие синергические (согласованно действующие) или антагонистические влияния на различные физиологические и патологические показатели. Скажем, пары: железо-марганец, железо-цинк, цинк-медь, кадмий-медь, медь-молибден и т.д.; триады: йод-кальций-остаток фосфорной кислоты, молибден-медь-остаток серной кислоты. Медь и марганец, являясь антагонистами молибдена, способствуют развитию выраженной формы его дефицита, который рассматривают как один из факторов предрасположенности к онкологическим заболеваниям. Низкий уровень селена в сыворотке крови указывает на снижение антиоксидант-ной защиты организма. Его антагонистами являются свинец, ртуть, кадмий, мышьяк. Известен механизм повреждающего действия перечисленных элементов, действующих как тиоловые яды. Возможен и другой путь: опосредованно через снижение уровня селена. Поэтому низкая его концентрация в сыворотке крови и повышенная в волосах может служить одним из тестов ранней диагностики токсического действия антагонистов селена. Но подтверждающий результат возможен только по совокупности данных многоэлементного анализа металлов и количественного определения клинически важных индикаторов их дисбаланса. При этом важна информация о содержании как можно большего числа искомых элементов в одной пробе одновременно и в различных типах биообъектов (например, в крови и волосах).
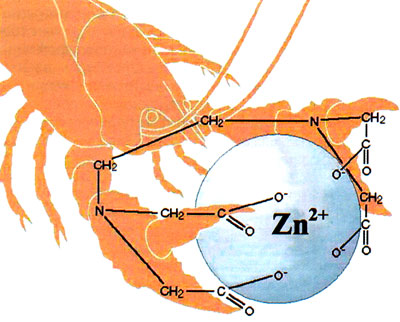
Большая часть металлов в организме находится в виде хелатов (клешневидных комплексов)
с биологически активными веществами
Организм — сложная динамическая полилигандная (Лиганды — в комплексных соединениях молекулы или ионы, связанные с центральным атомом (комплексообразователем)) и полиметаллическая система, для ее функционирования необходимо поддержание гомеостаза. Обмен, циркуляция, депонирование ионов металлов объясняются их способностью участвовать в процессах комплексообразования с природными эндогенными лигандами (нуклеиновыми кислотами, углеводами, аминокислотами, пептидами, белками, витаминами, гормонами) и экзогенными (лекарственными препаратами, пищевыми продуктами и др.). Нарушение же гомеостаза вызывается превалированием или дефицитом ионов металлов (допустим, изменение геохимической среды обитания, заболевание), увеличением или снижением концентрации лигандов (длительное применение ряда лекарственных средств, определенная диета).
Выступая в качестве центрального атома, большинство микроэлементов образуют биокомплексы in vivo. Их устойчивость играет фундаментальную роль во внутри- и внеклеточной динамике, антагонизме, синергизме и фармакодинамическом действии металлов. Большая их часть присутствует в организме в виде хелатов (Хелаты — комплексные соединения циклического строения, в которых лиганд соединен с центральным атомом металла посредством двух или большего числа связей) микроэлементов с биологически активными веществами.
Устойчивые комплексы постоянно находятся в организме и играют строго определенную функциональную роль: тот же гемоглобин, витамин В12, цитохромы (дыхательные ферменты). А непрочные комплексы образуются только для выполнения конкретных функций и после их завершения разрушаются. В таких случаях ионы металлов служат активаторами ферментов на период их каталитического действия. Например, в металлополинуклеотидных комплексах ионы марганца, кобальта, железа, никеля стабилизируют двойную спираль ДНК и могут заменять друг друга. Впрочем, устойчивость биокомплексов определяется многими факторами, наиболее важные из них — комплементарность (Комплементарность — взаимное соответствие в химическом строении двух макромолекул, обеспечивающее их взаимодействие. Комплементарные структуры подходят друг к другу как ключ к замку), природа микроэлементов и лигандов, меж- и внутримолекулярные взаимодействия, кинетика комплексообразования и др. Например, ионы меди (Cu), никеля (Ni +), кобальта (Со ) и цинка (Zn ) эффективно конкурируют с протонами за атом азота в азотсодержащих лигандах. Стерические (пространственные) особенности образуемых комплексов способствуют увеличению их проницаемости через клеточные мембраны и модулируют доступность для разнообразных клеточных рецепторов. Близкие же кинетические параметры формирования этих структур обусловливают наблюдаемый параллелизм в поведении ряда металлов (магния, марганца, кобальта, цинка, меди, ртути, свинца и др.).
Биокомплексы металлов представляют уникальную группу соединений, участвующих в поддержании целостности клетки. «Объединения» одного и того же биолиганда с различными ионами металлов могут характеризоваться несхожими биохимическими свойствами. Это объясняет множественность биологических эффектов таких комплексов. Разная степень сродства упомянутых ионов к тем или иным биолигандам может быть причиной их антагонизма. Белок металлотионеин содержит 61 аминокислотный остаток, способен связывать 7-10 атомов цинка, меди, кадмия, ртути, золота, серебра и тем предохраняет организм от интоксикации их ионами. В виде комплекса с металлотионеином осуществляется внутриклеточный транспорт двух антагонистов — меди и цинка. Последний еще и депонируется, т.е. временно выводится из процесса циркуляции. Ионы этих металлов стимулируют выработку металлотионеина, причем активность цинка более выражена, однако прочнее образующееся комплексное соединение с ионами меди. Повышение в организме концентрации ионов цинка вызывает выработку дополнительного количества металлотионеина, связывающего ионы меди, уменьшая тем их концентрацию в плазме. Другой пример. Некоторые вещества, присутствующие в пище, могут затруднять всасывание металлов. Так, ионы железа образуют прочные комплексы с полифенольными соединениями. Чай, кофе, соевый белок, содержащие такие структуры, значительно тормозят этот процесс.
В многоклеточном организме взаимодействие между клетками происходит не только механически, но и коммуникационно. И существует много механизмов обмена информацией между ними. Способность воспринимать внешние сигналы определяется рецепторами — специальным классом белковых молекул. Они имеют один или несколько центров связывания сигнальных молекул и проявляют высокое сродство к своим лигандам. Вступая в связь с рецептором, внеклеточные химические посредники воздействуют на протекание в клетке-мишени физиологически важных процессов. Во всех механизмах такого рода участвуют ионы металлов. Так, ионы кальция или цинка, как свидетельствуют исследования, служат посредниками множества важнейших клеточных реакций.
Как было показано выше, в силу различных обстоятельств возможна конкуренция между ионами металлов. Нарушение баланса внутриклеточных микроэлементов в организме, скажем, введение ионов из внешней среды (рекламируемые биодобавки, загрязненные солями металлов пища, вода, воздух и т.д.), может серьезно повлиять на работу системы, опосредующей внеклеточные сигналы различной химической природы.
АПОПТОЗ: ПРИЧИНЫ СБОЕВ
Постоянство количества клеток в организме поддерживается за счет их размножения и апоптоза — запрограммированной гибели. Металлы способны нарушать эту регуляцию, что усиливает мутацию и клональный рост. Микроэлементы вовлечены в самосборку и синтез митохондриальных ферментов, следовательно, в работу комплексов дыхательной цепи. Соли свинца, никеля, кадмия, ртути, некоторые другие экопатогены, обладающие генотоксическим действием и вызывающие дефекты ДНК, способны блокировать эти ферменты, что ведет к митохондриальной недостаточности. Усугубить эффект может как дефицит, так и избыток или дисбаланс ряда жизненно важных микроэлементов. В генной регуляции апоптоза важную роль играют его ингибиторы — белокЬс1-2, обладающий ан-тиоксидантными свойствами, действующий подобно ловушке для свободных радикалов, и белок р53. Так, апоптоз, индуцированный агентами, вызывающими разрывы ДНК (металлы, радиация), зависит от транскрипции именно р53. Ионы ряда металлов - никеля (Ni2+), свинца (РЬ +), кадмия (Cd +) и других - мот вызывать мутации или повреждение Rb-гена (супрес-сор опухолевого роста), что приводит к клонированию мутировавшей клетки. А хром, свинец, ртуть, кадмий усиливают генотоксические эффекты. Группы с участием селена, цинка, железа, меди препятствуют реалиации геноповреждающего действия. Поддержание лабильного уровня внутриклеточных микроэлементов — важнейший фактор гомеостаза, поскольку их дисбаланс опосредованно запускает механизм нарушения апоптоза. Разбалансировка может быть следствием неполноценного питания, социально-экономического неблагополучия, наличия в почвах и водах очень низкого или, наоборот, высокого содержания тех или иных микроэлементов, интоксикации, вызванной введением ксенобиотиков (ряда лекарственных препаратов, этанола или наркотиков). А еще — следствием непродуманных медико-профилактических мероприятий типа всеобщей йодной профилактики, «борьбы» с анемией, использованием в детских учреждениях мультиминеральных смесей с витаминами различных химических групп.
Нарушение процессов регуляции апоптоза может приводить к заболеваниям: повышенная его активация, связанная с функцией ионов кальция (Са2+) и магния (Mg2+), — звено патогенеза СПИДа, нейрогенеративных и ишемических заболеваний; ингибирование, вызываемое ионом цинка (Zn ), определяет опухолевые поражения различной природы, вирусные инфекции. Каждый канцерогенный металл, видимо, имеет уникальный механизм действия и специфичность путей поступления. Кадмий и 6-валентный хром онкогенны только при ингаляционном введении, а мышьяк и бериллий, помимо этого, еще и при пероральном и, возможно, дермальном проникновении.
Наши эксперименты на примере комплексов железа и кобальта с производными ряда лекарственных препаратов (лигандов) показали взаимосвязь между физиологическим действием металлов, их биокомплексов и изменением электронной структуры центрального атома. Микроэлементы, в зависимости от ближайшего лигандного окружения, значений рН среды, степени окисления, ионогенной или ковалентной формы нахождения в образце, по-разному действуют на клетку и опосредованно влияют как индукторы или ингибиторы регуляции апоптоза. Ионы кобальта (Со2+), подобно ионам железа (Fe +), индуцируют перекисное окисление липидов, подавляют репарацию ДНК, а также с ионами никеля (Ni +), свинца (РЬ2+), кадмия (Cd2+) обладают комутагенными (близкими и усиливающими) эффектами, запускают синтез противовоспалительного цитокина, вызывающего апоптоз и некроз клеток-мишеней.
Сегодня уже можно констатировать ряд фактов участия макро- и микроэлементов в процессах апоптоза. Разнообразные митохондриальные дефекты у пациентов с болезнью Вильсона-Коновалова (наследственным заболеванием, характеризующимся накоплением меди в печени) предполагают связь между уровнем обмена меди и стабильностью митохондриального генома. Накопление токсикантов (кадмия, ртути, свинца), избыточное высвобождение связанных жизненно важных микроэлементов (железа, кобальта, меди, селена) провоцируют генерацию активных форм кислорода, что ведет к увеличению потенциального риска повреждения генов опухоль-супрессирующих белков. Именно по этой причине происходит торможение апоптоза клеток, содержащих мутации, и развивается канцерогенез. Гемохроматоз (Гемохроматоз — генетическое нарушение, характеризующееся аномально высоким прохождением железа через клетки кишечника и накоплением его в таких тканях, как печень, сердце и поджелудочная железа, приводящее к их повреждениям) и болезнь Вильсона-Коновалова увеличивают риск рака печени из-за накопления мутантного белка.
В нашей стране в последнее время рост заболеваемости гемохроматозом связан с распространением наркотиков, алкоголизма и повсеместным употреблением пива в металлической упаковке. Установлена корреляция между повышенным содержанием железа в организме и ранним развитием атеросклероза, ишемической болезни, опухолей. С одной стороны, это жизненно-важный элемент, а с другой — его ионы (Fe" ), как индукторы перекисного окисления липидов, провоцируют разрывы ДНК, участвуют в мутагенезе и канцерогенезе. Железо in vivo находится в виде комплексов в составе трансферрина (Трансферрин — сложный белок, переносящий ионы трехвалентного железа в организме. Обнаружен в плазме крови, молоке, яичном белке. Недостаток приводит к нарушению обмена веществ) и ферритина (Ферритин — железосодержащий белок печени, селезенки, костного мозга и других тканей. Запасает железо в организме), обрывающих цепь дальнейших реакций повреждения генома. Согласно литературным и собственным данным, органические комплексы этого металла стабилизируют геном, однако в ионизированном состоянии он может вызывать повреждение ДНК и провоцировать смерть клетки.
Значительная часть населения Земли страдает заболеваниями, связанными с дефицитом жизненно важных микроэлементов. Скажем, недостаток железа и селена испытывают до 1 млрд человек, хрома — до 3, меди - от 3,6 до 3,8, цинка — до 4,5 млрд человек. Восстановление же баланса может оказаться тем «маленьким ключом, которым можно открыть большой сундук», где хранятся рецепты новых фармакотерапевтических способов лечения различных заболеваний, улучшения качества и увеличения продолжительности жизни при сохраненном интеллекте.
НОВЫЕ МЕТОДЫ ИЗМЕРЕНИЯ
Для обоснованных выводов о результатах патогенного действия химических ультрамикроимпульсов на организм человека необходима их диагностика на протяжении жизни целого поколения. Получить достоверные и надежные результаты при необходимости массовых исследований возможно в лабораториях, использующих совокупность чувствительных методов анализа, таких, как масс-спектрометрия с индуктивно-связанной плазмой, гамма-резонансная спектрометрия, газовая хроматография с масс-спектрометрией и т.д. Гамма-резонансные спектрометры, на наш взгляд, станут эффективным инструментом при создании банка эталонов идентификации и содержания различных форм железа, кобальта, олова в организме как в норме, так и при патологиях. Современная аппаратура позволяет одновременно определить в одной пробе 60 и более макро-, микро- и ультрамикроэлементов, что очень важно при оценке взаимовлияния и взаимодействия одних с другими у человека. К сожалению, высокая стоимость подобной техники пока тормозит ее внедрение. Для широкого применения новых аналитических методов в токсикологии целесообразно использовать отечественные высококачественные приборы, в том числе созданные в Институте аналитического приборостроения РАН (Санкт-Петербург).
В Российской Федерации нет пока четких указаний на обязательность элементного анализа при медико-диагностических исследованиях, хотя именно он стал бы важным инструментом поиска рациональных стратегий лечения хронических и опухолевых заболеваний. На сегодня число аккредитованных в соответствии с международными стандартами лабораторий для многоэлементного анализа биосубстратов еще крайне мало. Так, в Москве подобный статус из доступных для пациентов имеет только Центр биотической медицины профессора Анатолия Скального.
Установлено: более 80% употребляемых лекарственных препаратов, продуктов питания могут вступать в реакции комплексообразования с металлами in vivo, вызывая нарушение баланса микроэлементов клетки и связанные с этим патологии — микроэлементозы. Что такое норма в биологических пробах? Вовсе не обязательно она совпадает со средней величиной, а прежде всего основывается на оптимальности функции и отличном здоровье. Определить ее для переменной величины значительно труднее и важнее, чем некий средний показатель. Например, концентрация цинка в волосах падает в течение первых трех лет жизни ребенка, а хрома и кремния в некоторых тканях снижается на протяжении всей жизни. Известно, что легкие, кожу, ногти, волосы можно использовать в качестве индикаторов хронического воздействия микроэлементов. Имеющиеся данные показывают: содержание их в волосах отражает соответствующий статус организма в целом. Такие пробы — интегральный показатель минерального обмена.
Элементный анализ должен стать частью процедуры контроля качества субстанций, растительного сырья и других средств медицинского назначения. Допустим, в практике широко используют железосодержащие лекарственные вещества. Потеря активности и увеличение токсичности подобных препаратов при хранении характеризуется увеличением содержания доли трехвалентного железа по сравнению с двухвалентным. Методом гамма-резонансной спектрометрии можно определить различные формы железа, в том числе и степень его окисления в биологическом материале. Комплексное доклиническое изучение безопасности потенциальных лекарственных средств способно выявить большинство токсических и неблагоприятных побочных эффектов. И несмотря на опосредованный характер большей части биопроцессов, протекающих в организме при участии металлов, сегодня реально количественно оценить действие последних.
Лекарственные растения — важнейшие объекты экологического мониторинга. Способные к активному комплексообразованию микроэлементы могут присутствовать в таком сырье в виде различных соединений с углеводами, алкалоидами, полифенолами и т.д. Ведь известны некоторые растения, грибы и микроорганизмы, метаболические процессы в которых позволяют извлекать из почвы токсические металлы, что создает опасность их дальнейшего перемещения по пищевой цепи. Отдельные виды плесени можно культурировать при таких условиях, когда они будут восстанавливать ртуть в ионной форме до элементной ртути. А ее пары быстро диффундируют через клеточные мембраны. Аналогично «неорганический» свинец способен подвергнуться биотрансформации некоторыми бактериями до тетраэтилсвинца — органического вещества, транспортирующегося через биологические мембраны и весьма токсичного.
Многочисленные исследования показали: высокий уровень антропогенной нагрузки на систему «мать-
плод» приводит к дисбалансу микроэлементов в биосредах фетоплацентарного комплекса (обеспечивающего развитие плода). На основании результатов анализа содержания металлов в почве и питьевой воде на территории районов с различной степенью загрязнения и уровня накопления микроэлементов в плаценте и крови плода были выявлены соответствующие приоритетные экотоксиканты. Так, почвы Ярославской, Ивановской и сопредельных с ними северных областей России крайне бедны железом, а в Курской, западной части Московской области насыщены им. По-прежнему, как самые безопасные лекарственные средства, будущим мамам рекомендуют растительные сборы, но полный элементный их состав, согласно действующим нормативным документам РФ, не контролируется.
ДИСБАЛАНС МЕТАЛЛОВ И ЛИГАНДОВ
Онкологические и нейродегенеративные заболевания, атеросклероз, гипертония и другие «болезни цивилизации» с позиций молекулярной медицины имеют общие факторы риска. В их числе прежде всего — оксидативный стресс, связанный с генерированием в организме высокоактивных свободных радикалов и нерадикальных частиц с атомом кислорода или азота. Активные формы кислорода (АФК) выполняют двоякую функцию: позитивную (межклеточная сигнализация, фагоцитоз, выработка энергии и т.п.), однако в случае гиперпродукции — негативную (повреждение липидов мембран клеток, белков, углеводов, нуклеиновых кислот).
Ионы металлов, в частности двухвалентного железа и одновалентной меди, могут усиливать образование АФК, скажем, высокоагрессивного гидроксильного радикала ОН. Связывание этих ионов в комплекс существенно снижает скорость протекания свободнора-дикальных процессов. Биокомплексы цинка, меди, кобальта, железа, никеля ингибируют и многие другие ферменты, включенные в генерацию АФК или активных форм азота.
Селен, хром, марганец, цинк, кобальт, медь, железо и др. занимают ведущее место среди экзо- и эндоанти-оксидантов, но при условии их нахождения в координационно-связанной форме. Способность микроэлементов образовывать внутри- и межмолекулярные комплексы практически со всеми эндогенными ли-гандами становится определяющей при выяснении активности металлосодержащих лекарственных препаратов во избежание проявления их компонентами токсического влияния.
Рекомендации по использованию пищевых метал-лосодержащих добавок нередко подразумевают совет: «Чем больше, тем лучше». При этом игнорируют потенциальные токсические эффекты не столько от избыточного потребления микроэлементов, сколько от их формы (ионной или координационно связанной) в рекламируемом препарате. Между тем неблагоприятны эффекты и от их избытка. В высоких дозах они действуют как прооксиданты, генерирующие свободные радикалы, или как ингибиторы ключевых ферментов, включенных в метаболизм. Скажем, в развитии таких нейродегенеративных заболеваний, как болезни Альц-геймера, Паркинсона, этиологическую роль играют ионы алюминия, меди, кадмия, свинца. Действие фермента пироглутамил-аминопептидазы, участвующего в инактивации нейромедиатора — гамма-амино-масляной кислоты, подавляется низкими концентрациями перечисленных металлов; ионы железа, никеля, меди селективно нарушают процессы метаболизма другого нейромедиатора — дофамина. «Алюминиевая» энцефалопатия опосредованно приводит к значительному оксидантному стрессу в цитоструктуре нейрона. Ряд исследований последних лет показал: избыточный алюминий включается в трансферрин и занимает место железа. Кроме того, связывает ферритин, нарушая высвобождение железа, в результате возрастает окислительное повреждение тканей. Учитывая, что ключевым моментом в болезнях цивилизации служит нарушение баланса про- и антиоксидантных молекул в организме, применению металлосодержащих пищевых добавок, специальных диет, «безвредных» препаратов растительного происхождения должна предшествовать элементная диагностика пациента.
Предлагаемый нами способ коррекции дисбаланса микроэлементов основан на интегральном подходе к информации о динамике их содержания в организме при конкретной патологии, об изменении свойств металла и лиганда (лекарства) при комплексообразовании, о принципе «узнаваемости» мембранами клеток структур, близких по строению природным биомолекулам. Нами синтезировано и защищено патентами РФ более 100 новых веществ, построенных по принципу биокоординационных и азот-гликозилированных структур цинка, кобальта, меди, никеля, железа, марганца с лекарственными средствами. В экспериментах подтверждена бактерицидная и бактериостатическая, антиоксидантная, иммуномодулирующая, противовоспалительная, ранозаживляющая, радиопротекторная активность созданных препаратов. Мы установили их способность восстанавливать баланс микроэлементов и металло-лигандный гомеостаз.
Оптимальный же вариант лечения можно выбрать на основе индивидуальной элементограммы пациента, что позволяет считать биокомплексы микроэлементов новой генерацией лекарств. Сведения об изменении элементного статуса организма при патологических состояниях исключительно важны, но до настоящего времени разрознены и еще малодоступны для практики в РФ. Впрочем, уже в ближайшие 2-3 года технически станет возможной реализация ряда задач персонализированной медицины, например, генетический паспорт человека. По-видимому, определение концентрации металлов, коррелирующих с генетической информацией ДНК, станет выполнимым и в нашей стране. Таким образом, понятия дефицита, избытка и дисбаланса микроэлементов будут иметь строго аналитический характер.
Доктор биологических наук Наталья КАЛЕТИНА,
кандидат медицинских наук Григорий КАЛЕТИН, Центр биотической медицины (Москва)
кандидат медицинских наук Григорий КАЛЕТИН, Центр биотической медицины (Москва)
"Наука в России", № 1, 2007





 Издательство «Свиньин и сыновья» выпустило несколько сотен самых разных по жанру, объему и авторам, но неизменно высококультурных изданий
Издательство «Свиньин и сыновья» выпустило несколько сотен самых разных по жанру, объему и авторам, но неизменно высококультурных изданий





